
La clase Heliobacterias (Orden Heliobacteriales, Phyllum Firmicutes), corresponde a un grupo muy especializado de bacterias fotoheterótrofas Gram+.
Descrito por primera vez en 1983 por Ghest y colabordores [3], a la fecha tiene definidos dos clados, cuatro géneros (Heliobacterium, Heliobacillus, Heliophilum y Heliorestis) y diez especies.
Las especies son mayormente terrestres, raramente acuáticas, anaerobias estrictas, prosperando en suelos anóxicos, muchas veces asociadas en relaciones mutualistas con cultivos de arroz, y al igual que las especies heterótrofas del grupo, presentan endosporulación. Algunas especies (Heliobacillus movilis, Heliobacterium modesticalium) han sido reportadas en suelos proximos a fuentes termales. H. modesticalium, hallada Islandia, ha sido una de las especies mejor estudiadas.
Considerado a nivel bioquímico un grupo minimalista, exhibe el aparato bioquímico de captura de energía mas simple dentro de todos los grupos bacterianos fototrófos y fotosintéticos reportados a la fecha. Su hallazgo ha aportando significativamente al entendimiento de la evolución de la fotosíntesis, se considera un grupo muy primitivo, con razgos bioquímicos ancestrales conservados.
Las Heliobacterias son incapaces de fijar carbono a partir de CO2, por lo que se considera un grupo bacteriano fotoheterótrofo, no fotosintético. Dependiendo de las condiciones ambientales, utilizan distintos compuestos como fuentes de electrones: H2S y compuestos orgánicos en suelos alcalinos, Fe2+, H2, succinatos y piruvatos en ambientes reductores y ácidos orgánicos en aguas termales.
CAPTURA DE ENERGÍA
A diferencia de los demás grupos bacterianos fotótrofos, las Heliobacterias no presentan complejos antena exclusivos a la función de captura de energía lumínica.
Su centro de reacción, HbRC, integra en un solo complejo las funciones de captura de energía y tránsito ETC, con dos dominios claramente diferenciables para cada una de las funciones: Dominio antena y dominio RC.
ESTRUCTURA PROTEÍNICA
El complejo HbRC corresponde a un homodimero con simetría C2, 24 hélices transmembrana (TMHs) de las cuales 22 están asociadas al homodímero PshA y dos recientemente descritas a una nueva subunidad PshX, ver Fig.1 A. La distribución de pigmentos se describe en la Fig.1 B.
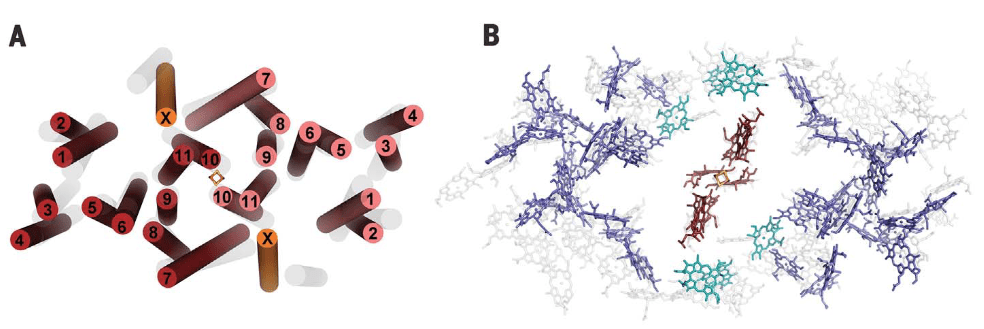
Figura 1. Arreglo de hélices Transmembrana (TMHs y pigmentos) en HbRC. Vista superior. Fuente: Gisriel et.al., 2017. En las imagenes, el autor superpone en gris las hélices (Fig A) y pigmentos (FigB) correspondientes a TMHs de PSI de plantas superiores.
DOMINIO ANTENA
El core del Dominio Antena corresponde a 54 bacterioclorofilas Bchl g (pigmentos de color azul) distribuidas en dos capas, ver Fig 2. De las 54 Bchl g, seis (azul intenso) son proximales al dominio RC, siendo probablemente las unidades responsables de la exitación del par especial de clorofilas.
Es importante resaltar que Gchl g , un isómero de Chl a, solo está presente en este grupo bacteriano.
En adición a las 54 Bchlg, cuatro Bchl g´ adicionales estan coordinadas por las subunidades Pshx (pigmentos magenta) igualmente proximales a RC. Bchl g´es un esteroisómero de Bchl g.
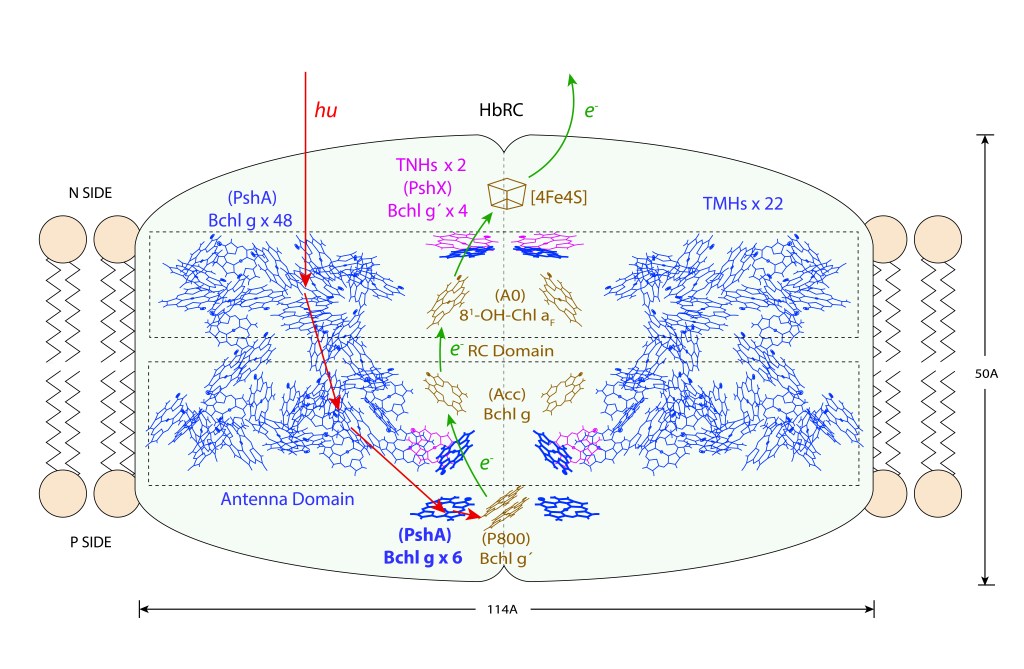
Figura 2. Heliobacterias: Estructura y dinámica general del complejo HbRC. Nota: La distribución y número de pigmentos en PshA es solo ilustrativo. para información mas rigurosa consultar Gisriel et.al., 2017.
En adición a los pigmentos mencionados, dos moléculas de naturaleza lipídica y dos carotenos 4,4´ Diaponeurosporeno, uno por sumbunidad mioonodimérica, forman parte del Dominio Antena, ver Fig.3.
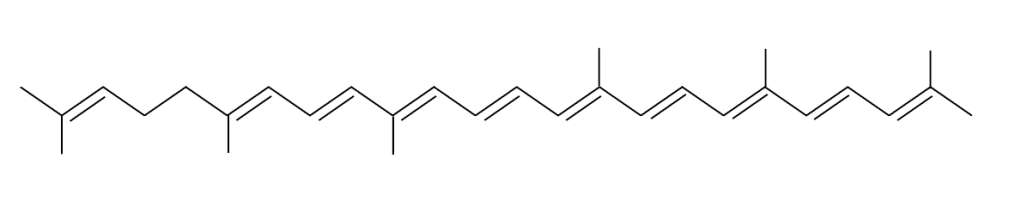
Figura 3. Estructura molecular C30 4,4´ diaponeurosporeno
DOMINIO RC
La ruta de transferencia electrónica (ETC) en Heliobacterias es similar a la de bacterias verdes del azufre, si bien la frecuencia de exitación es mucho más baja, ubicandose en el infrarojo cercano, alrededor de 798-800 nm. ver Fig.4.
En heliobacterias, P800 corresponde a Bchl g´, Acc a Bchl g y A0 a la clorofila 81-OH-Bchl aF.
La energía es finalmente entregada a una Fx del tipo [4Fe 4S] para luego reducir NAD+ a su forma NADH, mediante un intermediario FeS A/B.
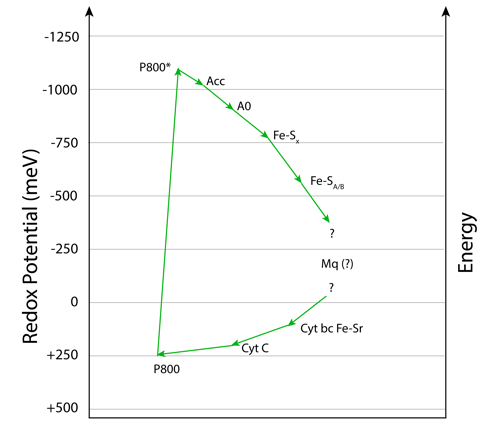
Figura 4. Heliobacterias: Ruta de transferencia electrónica.
POOL DE QUINONAS
El pool de quinonas está representado por menaquinonas. En ausencia de un complejo II que pueda aportar directamente quinonas reducidas al pool, la enzina NDH puede estar soportando este rol, con NADH como fuente aportante de electrones.
CITOCROMO BC
Similar en función a los citocromos BC1 y B6f, realizan en este caso un flujo cíclico, con electrones transportados por un Cyt C soluble hacia el fotosistema, contribuyendo al aporte de electrones.
METABOLISMO REDUCTOR
Como ruta reductora, las Heliobacterias disponen de un ciclo parcial r-TCA . Dada la la ausencia de genes codificantes de ATP-Citrato Lyasa, el piruvato requerido por el ciclo debe ser obtenido por rutas anapleróticas, cedido por las plantas hospederas o a partir del sustrato.
Al igual que en GSB, los Ciclos CBB y Biciclo 3-HP están ausentes. En general las rutas bioquímicas del carbono aparecen muy simplificadas en Heliobacterias. En contraste, las rutas fijadoras de nitrógeno (Mo dependientes) son muy robustas. En este sentido podrían desempeñar en gramineas un soporte nitrificante similar al de Rhizobium, Bradyrhizobium y Sinorhizobium en leguminosas, si bién nunca conformando nódulos radiculares.
Puesto que son un grupo Gram+ carente de membrana interna, el espacio periplasmático desempeña la función del lúmen thylakoidal de cyanobacterias y del espacio intermembrana de bacterias púrpura, lo que les permite confinar el H+ requerido para la síntesis de ATP.
Como se mencionó anteriormente, la enzima transmembrana NDH (NADH-MQ Oxidoreductasa) forma parte de la bioquímica del complejo jugando un rol doble, transporte H+ hacia el espacio periplasmático y reducción de menaquinonas, lo que debe incrementar de manera significante la producción de ATP, ver Fig 5.
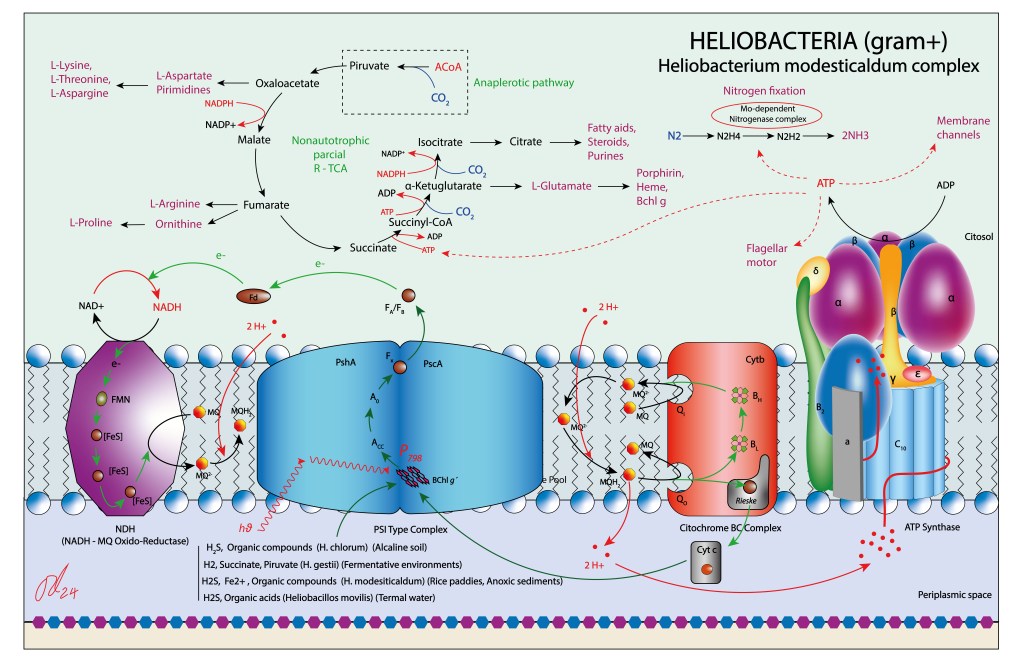
Figura 5 . Aparato fototrófico propio de Heliobacterias.
BIBLIOGRAFÍA RECOMENDADA
[1] Asao M, Madigan MT. Taxonomy, phylogeny, and ecology of the heliobacteria. Photosynth Res. 2010 Jun;104(2-3):103-11. doi: 10.1007/s11120-009-9516-1. Epub 2010 Jan 22. PMID: 20094790.
[2] Gisriel. C., Sarrou, I., Ferlez, B., Golbeck, J, J.H., Redding, K.E., and Fromme, R. (2017) Structure of a symmetric photosynthetic reaction center–photosystem. Science. 357:1021-1025
[3] Gest H. Discovery of the heliobacteria. Photosynth Res. 1994 Jul;41(1):17-21. doi: 10.1007/BF02184140. PMID: 24310008.
[4] Sattley WM, Blankenship RE. Insights into heliobacterial photosynthesis and physiology from the genome of Heliobacterium modesticaldum. Photosynth Res. 2010 Jun;104(2-3):113-22. doi: 10.1007/s11120-010-9529-9. Epub 2010 Feb 4. PMID: 20130998.
[5]Sattley WM, Madigan MT, Swingley WD, Cheung PC, Clocksin KM, Conrad AL Dejesa LC, Honchak BM, Jung DO, Karbach LE, Kurdoglu A, Lahiri S, Mastrian SD, Page LE, Taylor HL, Wang ZT, Raymond J, Chen M, Blankenship RE, Touchman JW 2008. The Genome of Heliobacterium modesticaldum, a Phototrophic Representative of the Firmicutes Containing the Simplest Photosynthetic Apparatus. J Bacteriol 190:. https://doi.org/10.1128/jb.00299-08
