SEM en falso color de Gemmatimonas phototrophica. (Jason Dean/Czech Academy of Sciences)
El hallazgo más reciente de bacterias fototróficas, (Zehg et. al., 2014), corresponde a la especie Gram-negativa Gemmatimonas phototrophica, una inusual bacteria fotoheterótrofa facultativa incapaz de fijar carbono a partir de CO2, que crece igualmente bién en obscuridad, de manera que la fotofosforilación complementa la fosforilación oxidativa.
Perteneciente al phillum Gemmatimonodota, fué colectada por primera vez en un lago al occidente del desierto de Gobi, siendo el primer reporte del grupo con evidencia de fotosíntesis anoxigénica.
Tras realizar el estudio genómico correspondiente, Zehg et. al, op. cit, identificaron un Cluster fotosintético completo (PGC) cuyo análisis comparativo con otras especies microbianas sugirió una adquisición temprana via transferencia horizontal desde una bacteria púrpura fotosintética, ver fig 1.
Éste hallazgo es la primera evidencia de transferencia horizontal fototrófica entre phyla bacterial distante, lo que proporciona nuevos y valiosos elementos a tener en cuenta en la evolución de la fotosintesis microbiana.
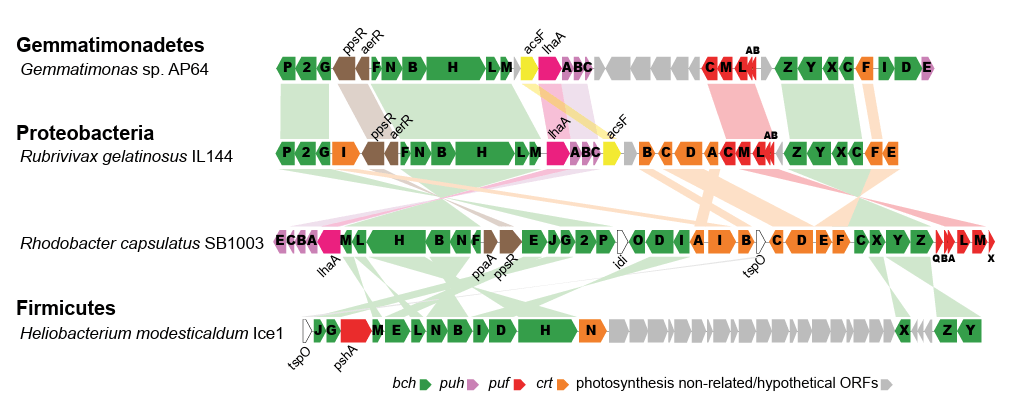
Figura 1. Referenciación genética del PGC de AP64 comparado con Proteobacterias (Rubrivivax gelatinosus y Rhodobacter capsulatus), y Firmicutes (H. modesticalum). Nótese la coincidencia particularmente con R. gelatinosus. Fuente: Zeng et.al. 2014: http://www.pnas.org/cgi/doi/10.1073/pnas.1400295111
Con éste nuevo encuentro ya son siete los grupos bacterianos fotosintetizadores descritos a la fecha: Cyanobacterias, Proteobacterias alfa y gamma (purpura no sulfurosa y sulfurosa respectivamente), Chlorobi (GSB) , Chloroflexi (FAP) , Firmicutes (Heliobacterias) , Acidobacteria y finalmente Gemmatimonadetes (Gemmatimonas).
El complejo LHC/RC, denominado en este grupo RC-dLH precenta una pseudosimetría C8, con el complejo antena (LHC) de anillo doble rodeando el centro de reacción (RC).
COMPLEJO ANTENA LHC
LHC está constituido por dos anillos concéntricos de corte ligéramente elipsoidal. El anillo interno, LH1, similar al complejo LHC de bacterias púrpura, recibe energía lumínica del anillo externo y la transmite al centro de reacción. El anillo externo, LHh, es responsable de capturar la energía solar y transmitirla a los pigmentos de anillo interno. ver Fig.1.

Figura 1. Estructura general del complejo RC-dLH. Se excluyen en la figura los pigmentos responsables de la cadena de transporte de electrones en el centro de reacción.
ANILLO INTERNO
El anillo interno, de estructura cilíndrica, es similar al complejo LHI de bacterias púrpura,está conformado por 16 unidades heterodiméricas de polipéptidos transmembrana α/β , α internas, β externas al anillo. Entre las subunidades α y β de cada heterodímero se ligan no covalentemente un par de pigmentos BChl a y un all-Trans carotenoide, Gemmatoxanthina, con bandas de absorción entre 400 y 600 nm, picos a 478, 507 y 542 nm. (Zehg et. al., 2014).
El par Bchl, B868a/B868b, absorbe energía a 868 nm, sus planos tetrapirrólicos son perpendiculares a la superficie citoplasmática, plano XZ, ver fig.2, y su posición es distal al centro RC. El caroteno, con orientación radial al complejo, atravieza el complejo de distal a proximal, tiene función fotoprotectora y de captura y transmisión de energía a las Bchl, ver Fig.2.
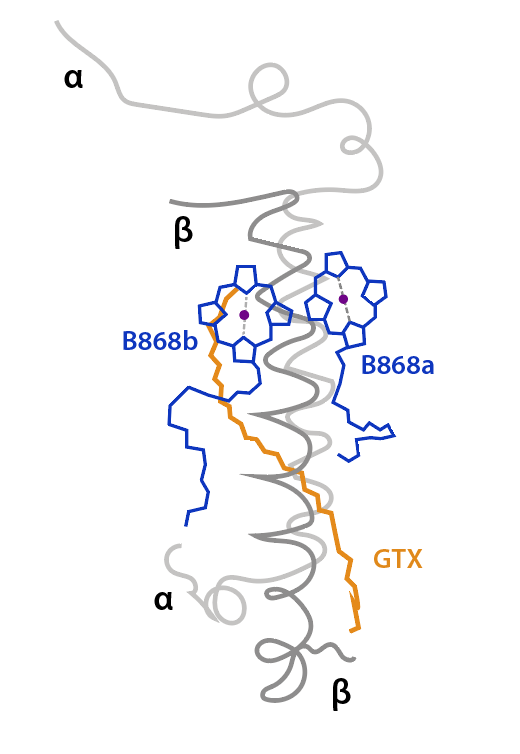
Figura 2. Unidad heterodimérica y pigmentos asociados al anillo LH1. Simplificado de Quian et.al., 2022.
ANILLO EXTERNO
El anillo externo, cónico, denominado LHh, está conformado por 24 heterodímeros polipeptídicos α/β, cada uno con un par de clorofilas BChl B816 en posición distal, alineadas en el plano XZ, una clorofila BChl B800 proximal alineada en el plano YZ, y un caroteno GTX radial atravezando el complejo, de manera similar a su posición en LH1, quedando en consecuencia los tres BChl con sus planos tetrapirrólicos perpendiculares al plano XY de la superficie citoplasmática. ver Fig.3.
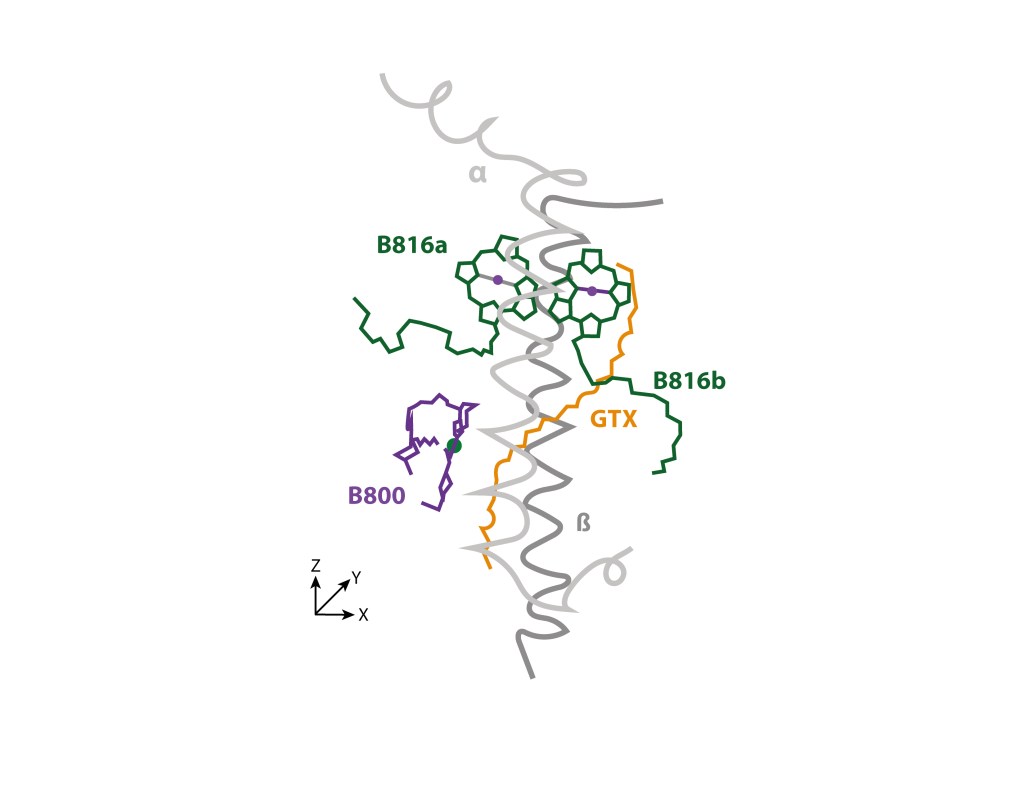
Figura 3. Unidad heterodimérica y pigmentos asociados al anillo LHh. Simplificado de Quian et.al., 2022.
La Fig 4. representa la transferencia de energía entre y dentro de los dos anillos LH1 y LHh. Los numeros representan los tiempos de transición entre estados, medidos en picosegundos. Aunque no está referenciado en la literatura, las transferencias electrónicas deben obedecer a resonancia no radiativa de Förster.
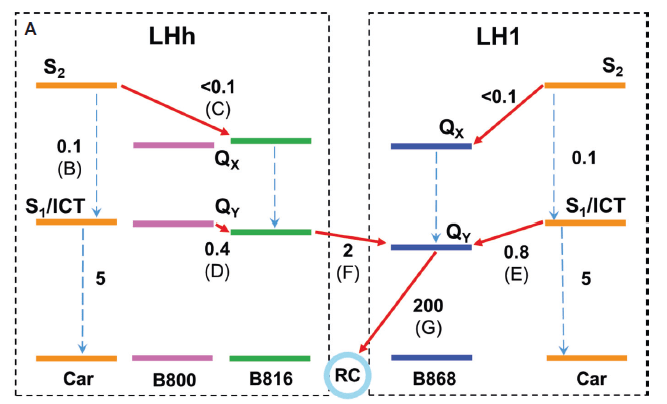
Fig 5. Cinética de transferencia de energía en el complejo RC-dLH1. Flechas rojas representan canales de transferencia de energía, líneas punteadas corresponden a procesos de conversión interna (IC). En GTX, S2 corresponde al segundo estado de singlete, S1/ICT al estado exitado mixto primer singlete/Intramollecular charge Transfer. En BChl´s, Qx y Qy corresponden a los estados exitados propios de este tipo de pigmentos.
CENTRO DE REACCIÓN RC
La arquitectura general del centro de reacción del grupo es similar al presente en proteobacterias fototróficas, ver lectura de bacterias púrpura, con un heterodímero principal conformado por las subunidades L y M y un citocromo c soluble responsable del transporte cíclico de electrones desde el citocromo BC1 hasta RC. En cuanto a otros elementos del complejo, la subunidad H se encuentra fragmentada en un polipéptido pequeño transmembrana (~7.7 kDa) y un segundo polipéptido de mayor tamaño, (~19.9 kDa), Hc, ubicado en el lado citoplasmático del complejo [3].
La Figura 4 resume el complejo fototrófico de este nuevo grupo.
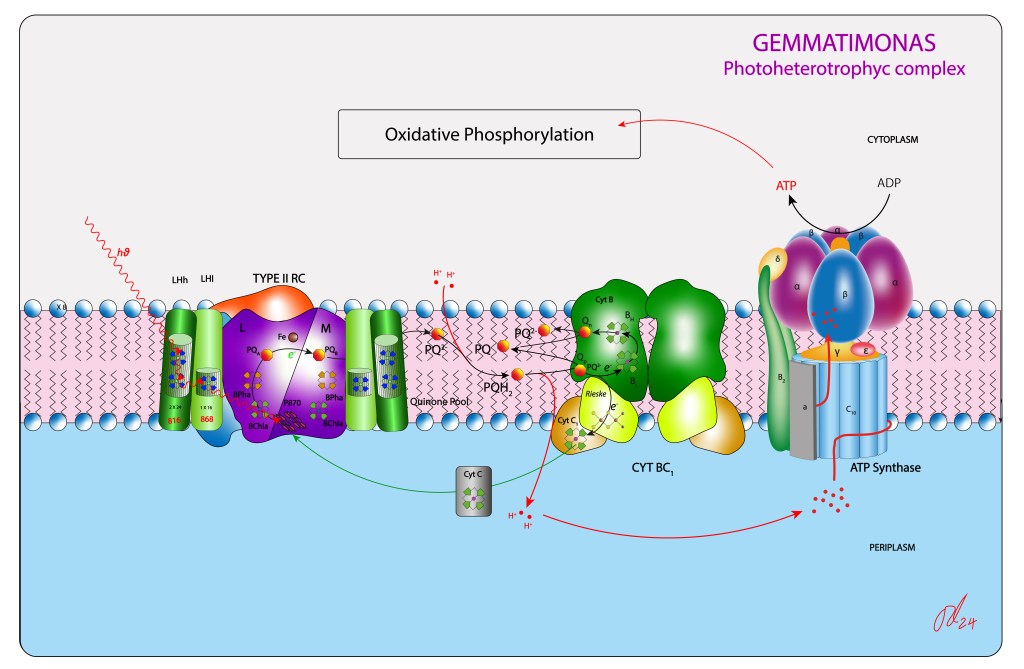
Figura 4. Aparato fototrófico en Gemmatimonas
METABOLISMO
Como se mencionó anteriormente, la transferencia horizontal de un plásmido proveniente de bacterias púrpura fotosintéticas fué seguramente el elemento responsable de la adquisición de la maquinaria fototrófica en la especie en estudio.
Sin embargo, la transferencia no involucró el genoma responsable de otras piezas requeridas para una función fototrófica completa. Así, en la especie no se ha evidenciado presencia de sistemas de captura de electrones desde moléculas donoras, orgánicas o inorgánicas, de manera que la función fototrófica depende exclusivamente de la retroalimentación cíclica de electrones desde el citocromo bc1 hacia el centro de reacción con cyt c como transportador cíclico. Adicionalmente, no se han evidenciado tampoco rutas reductoras asociadas a la cadena fototrófica, tipo ciclo reverso TCA, ruta reductora de las pentosas, ciclo del hidroxypropianato, etc, vías metabólicas características de los demás grupos bacterianos fototróficos, de manera que el ATP, producto final del complejo adquirido, alimenta directamente el complejo responsable de la fosforilación oxidativa. Esta nueva ruta alterna de síntesis de ATP le permite a la especie ahorrar moléculas orgánicas donoras de carbono en presencia de luz.
En cuanto al aporte del complejo LHC/RC a la función respiratoria, Koblízek et.al, 2020 resaltan varios puntos:
- Exposición de irradiancia lumínica de 100 μmol de fotones m-2 S-1 incrementó el crecimiento de las colonias bacterianas en aproximadamente un 30% , lo que sugiere que el complejo bioquímico adquirido optimiza la captura de energía durante exposición directa a la radiación solar.
- La exposición a radiación solar mejoró igualmente la asimilación de compuestos orgánicos. Así, a intensidades por encima de 400 μmol de fotones m-2 S-1 , la asimilación de glucosa fué 2.77 veces mayor que la la obtenida en obscuridad.
- No se evidencian mecanismos adaptativos a la luz, de modo que se produce la misma cantidad de complejos PS tanto en luz como en obscuridad.
- En contraste con otras bacterias anoxigénicas fototróficas que crecen aeróbicamente y sintetizan BChl a solo en obscuridad, la especie en estudio no crece bajo condiciones totalmente aeróbicas y produce BChl a incluso bajo luz contínua.
- En conclusión, G. phototrophica es un fotoheterótrofo típico facultativo, utiliza carbono orgánico para su biomasa y metabolismo, pero la luz mejora significativamente su crecimiento.
Finalmente, el hallazgo de la especie demuestra la capacidad bacteriana de importación via transferencia horizontal de genomas de función completa, lo que abre nuevas posibilidades para entender la evolución bacteriana. Para ilustrar el alcance del hallazgo, la presencia de dos complejos fotosintéticos PSI y PSII complementarios en cyanobacterias se ha explicad bajo la teoría de duplicación, evolución y diferenciación interna de los dos complejos fotosintéticos en una especie bacteriana para una posterior combinación evolutiva de los dos complejos en una sola maquinaria altamente eficiente.
El hallazgo abre otras posibilidades, con evolución a partir de transferencias horizontales interespecíficas, eventualmente interphila, entre donor PSII (o PSI) a aceptor con la contraparte complementaria.
BIBLIOGRAFÍA CITADA Y SUGERIDA
[1] P. Qian et al., 2.4-Å structure of the double-ring Gemmatimonas phototrophica photosystem. Sci. Adv. 8, eabk3139 (2022)
[2] R. E. Blankenship, Molecular Mechanisms of Photosynthesis (John Wiley & Sons, ed. 2, 2014), pp. 312.
[3] P. Qian, C. A. Siebert, P. Y. Wang, D. P. Canniffe, C. N. Hunter, Cryo-EM structure of the Blastochloris viridis LH1–RC complex at 2.9 Å. Nature 556, 203–208 (2018)
[4] Y. Zeng, F. Y. Feng, H. Medová, J. Dean, M. Koblížek, Functional type 2 photosynthetic reaction centers found in the rare bacterial phylum Gemmatimonadetes. Proc. Natl. Acad. Sci. U.S.A. 111, 7795–7800 (2014).
[5] Yurkov VV, Beatty JT Aerobic anoxygenic phototrophic bacteria. Microbiol Mol Biol Rev (1998) 62(3):695–724.
[6] M. Koblízek, M. Dachev, D. Bína, Nupur, K. Piwosz, D. Kaftan, Utilization of light energy in phototrophic Gemmatimonadetes. Journal of Photochemistry & Photobiology, B: Biology 213 (2020) 112085
[7] M. Dachev, D. BõÂna, R. Sobotka1, L. MoravcovaÂ, Z. Gardian, D. Kaftan, V. louf, M. Fuciman, T. PolõÂvka, Mi KoblõÂzÏek, Unique double concentric ring organization of light harvesting complexes in Gemmatimonas phototrophica. journal.pbio. (2017) 2003943
